Dans le cadre du projet MOISE, nous synthétisons, caractérisons et déterminons l’activité OER de nanoparticules IrOx supportées sur des aérogels d'oxydes métalliques (MOx). Pour acquérir des connaissances fondamentales sur les premiers stades de formation des oxydes de surface sur Ir, nous utilisons des monocristaux et combinons électrochimie à la spectroscopie d'impédance électrochimique, la spectroscopie de photoélectrons X et la spectrométrie de masse couplée à un plasma inductif. Nous avons récemment montré que les couches d'oxy-hydroxydes qui se forment dans la région avant l'OER présentent des états d'oxydation mixtes (présence d'espèces Ir(0), Ir(+III) et Ir(+IV)), et que la fraction de chaque état d'oxydation dépend de l'orientation cristallographique du monocristal Ir(hkl). Dans la région de l’OER, nos travaux fournissent des preuves que les espèces Ir(+III) se dissolvent progressivement, ce qui entraîne un enrichissement de la surface et des régions proches de la surface en espèces Ir(+IV), et donc une diminution de l'activité OER intrinsèque. Les résultats indiquent une convergence vers un état de surface plus stable mais moins actif, qui ne dépend ni de la disposition initiale des atomes de surface (orientation cristallographique, proportion d'atomes fortement et faiblement coordonnés) ni de leur état d'oxydation (état initial vs surfaces Ir(hkl) électrochimiquement activées). Pour en savoir plus.
En collaboration avec Bruno Gilles, directeur de recherche au SIMAP, nous élaborons également des couches minces d'Ir recouvrant un métal de transition moins cher et plus abondant (comme le cobalt (Co), le nickel (Ni), le cuivre (Cu), le fer (Fe) ou le Ru) par dépôt physique en phase vapeur. Ces couches minces servent à identifier les mélanges élémentaires appropriés, à étudier les conditions de recuit thermique et d'oxydation les plus appropriées (pression partielle, température) et la technique de dépôt pour obtenir des catalyseurs bimétalliques hautement actifs pour l’OER. Nous transférons ensuite les connaissances acquises sur électrodes modèles (monocristaux et films minces) à des nanoparticules IrOx. Dans ce but, nous développons des supports conducteurs électroniques qui (i) présentent une grande surface spécifique pour maximiser la distribution et éviter leur agglomération/agrégation, (ii) présentent une distribution optimale de la taille des pores pour permettre un accès facile des molécules d'eau à l'électrode et le transport du dioxygène produit et (iii) sont capables de supporter un potentiel électrochimique élevé (E > 1,7 V vs. l’électrode standard à hydrogène - SHE), une température moyenne (60 < T < 80°C) et un environnement très acide. Ces conditions de fonctionnement rendent instables les supports classiques à grande surface, tels que les noirs de carbone (le carbone est oxydé à des potentiels supérieurs à 0,207 V par rapport à la SHE). Nous nous concentrons sur les aérogels de SnO2 dopés, et modulons leur conductivité électronique en modifiant la nature et la concentration de l'élément dopant. Pour en savoir plus.
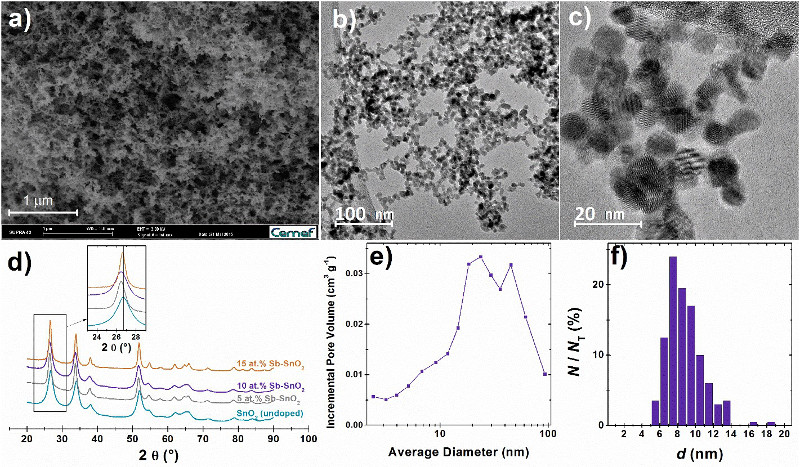
En combinant microscopie électronique à transmission, spectroscopie photoélectronique des rayons X et techniques électrochimiques, nous mettons en évidence des relations complexes entre la structure et la composition chimique des différents nanocatalyseurs, la nature du matériau de support et l'activité OER initiale et à long terme. Quelle que soit la chimie du nanocatalyseur initial, nous montrons que les espèces Ir(0) et Ir(III) sont progressivement oxydées en espèces Ir(V) et que la concentration de groupes hydroxyles et de molécules d'eau augmente continuellement en conditions OER. En revanche, aucun changement de l’état d'oxydation moyen, aucun changement du taux de recouvrement en groupements hydroxyle/eau et une activité OER constante sont observés sur les particules d'IrO2 de taille micrométrique. Nos résultats suggèrent donc que l'augmentation progressive de la fraction d’Ir d’état oxydation (+IV) associée à la diminution du nombre de nanoparticules isolées contribue à la baisse de l'activité spécifique OER dans des conditions pratiques de fonctionnement des anodes PEMWE. Pour en savoir plus.
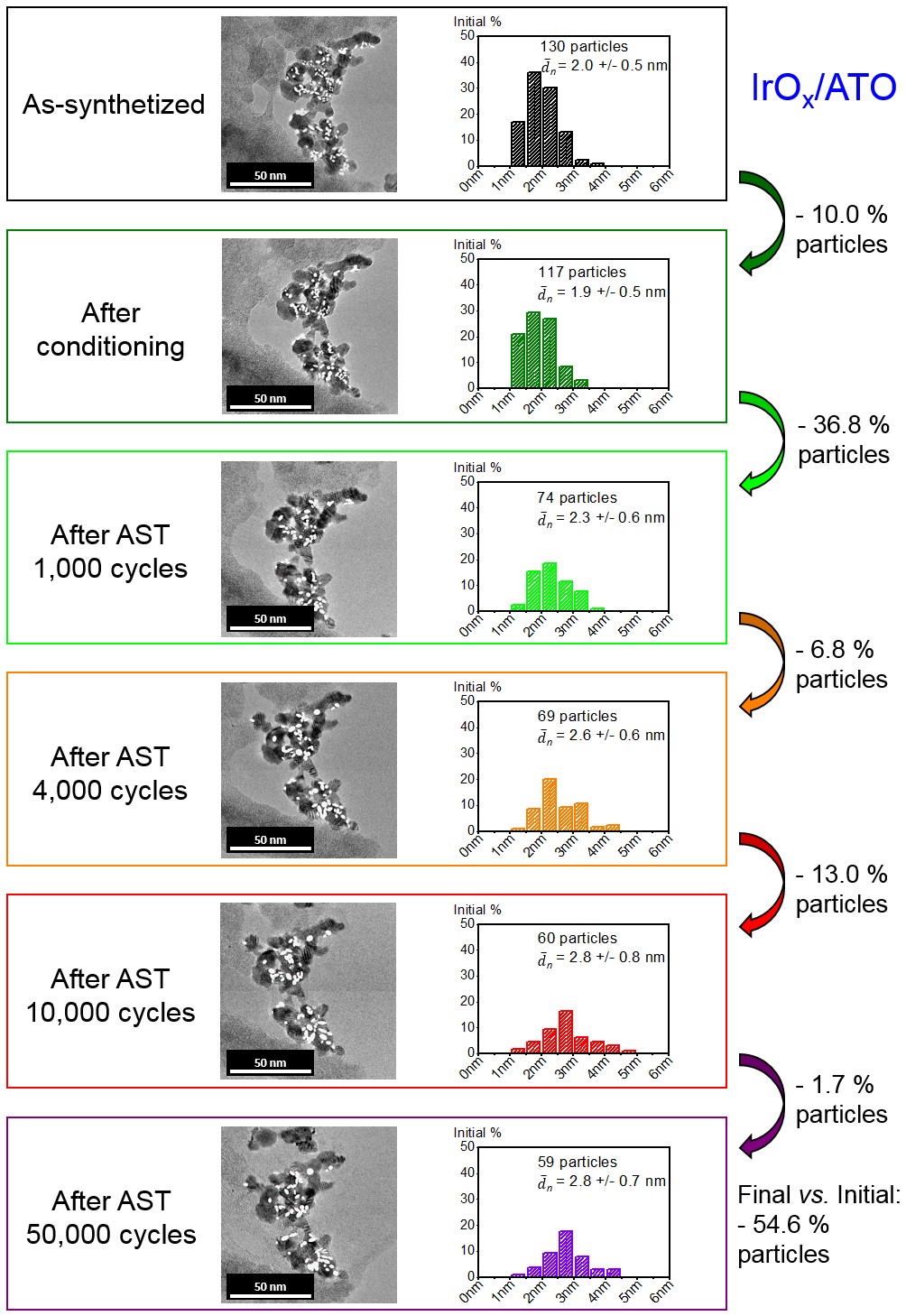
Au-delà de l'amélioration de l'activité pour l’OER, un autre de nos objectifs est de développer des méthodologies expérimentales permettant de déterminer in situ quelle fraction du courant est utilisée pour l’OER et quelle fraction contribue à la dissolution des nanocatalyseurs métalliques (Ir, oxydes d'Ir ou noyau riche en M, Irx+ + ions My+). Pour déterminer la sélectivité des nanocatalyseurs synthétisés, nous déterminons la quantité de métaux dissoute par spectrométrie de masse à plasma inductif (ICP-MS), un outil analytique capable de détecter les traces (parties par milliard) des éléments dissous en solution. Cette technique permet d'obtenir en temps réel la concentration des métaux dans l'électrolyte et d’étudier l'influence de divers paramètres opérationnels (pH, température, fenêtre potentielle, etc.).
Remerciements
Ce travail utilise les moyens de caractérisation mis en place par le Centre d’Excellence des Matériaux Architecturés Multifonctionnels "CEMAM" n° AN-10-LABX-44-01. Nous remercions l’Agence Nationale de la Recherche pour le financement du projet MOISE (ANR-17-CE05-0033).
Contact
Frédéric Maillard
Références
1. M. Scohy, S. Abbou, V. Martin, B. Gilles, E. Sibert, L. Dubau, F. Maillard, “Probing Surface Oxide Formation and Dissolution of Ir Single Crystals via X-ray Photoelectron Spectroscopy and Inductively-Coupled Plasma Mass Spectrometry”, ACS Catal. 9 (2019) 9859-9869. DOI: 10.1021/acscatal.9b02988.
2. M. Scohy, C. Montella, F. Claudel, S. Abbou, L. Dubau, F. Maillard, E. Sibert, S. Sunde, “Investigating The Oxygen Evolution Reaction on Ir(111) Electrode in Acidic Medium Using Conventional and Dynamic Electrochemical Impedance Spectroscopy“, Electrochimica Acta 320 (2019) 134536. DOI: 10.1016/j.electacta.2019.07.047.
3. L. Solà-Hernández, F. Claudel, F. Maillard, C. Beauger, “Doped tin oxide aerogels as Oxygen Evolution Reaction catalyst supports”, Int. J. Hydrogen Energy. 44 (2019) 24331-24341. DOI: 10.1016/j.ijhydene.2019.07.152.
4. F. Claudel, L. Dubau, G. Berthomé, L. Sola-Hernandez, C. Beauger, L. Piccolo, F. Maillard, “Degradation Mechanisms of Oxygen Evolution Reaction Electrocatalysts: A Combined Identical-Location Transmission Electron Microscopy and X-Ray Photoelectron Spectroscopy Study”, ACS Catal. 9 (2019) 4688-4698. DOI: 10.1021/acscatal.9b00280.
5. S. Watzele, P. Hauenstein, Y. Liang, J. Fichtner, S. Xue, B. Garlyyev, D. Scieszka, F. Claudel, F. Maillard, A. S. Bandarenka, “Determination of the Real Electroactive Surface Area of Ni-, Co-, Fe-, and Ir-based Oxide Electrocatalysts “, ACS Catal. 9 (2019) 9222-9230. DOI: 10.1021/acscatal.9b02006.



